Los altibajos científicos de los cannabinoides
En la actualidad existen cientos de estas sustancias químicas relacionadas con el cannabis, tanto naturales como sintéticas, que inspiran a los investigadores a ir en busca de avances médicos —y alimentan una peligrosa tendencia al consumo recreativo—.
Manténgase informado
Suscríbase al boletín de noticias de Knowable en español
Nota del editor: Raphael Mechoulam falleció el 9 de marzo de 2023, a los 92 años.
Los años sesenta fueron una gran década para el cannabis: las imágenes del flower power, el verano del amor y Woodstock no estarían completas sin un porro colgando de la boca de alguien. Sin embargo, a principios de los años sesenta, los científicos sabían sorprendentemente poco sobre la planta. Cuando Raphael Mechoulam, entonces un joven químico treintañero del Instituto Weizmann de Ciencias de Israel, se puso a buscar productos naturales interesantes para investigar, vio una tentadora laguna en los conocimientos sobre la hierba hippie: la estructura química de sus principios activos aún no se había descifrado.
Mechoulam se puso manos a la obra.
El primer obstáculo fue conseguir cannabis, ya que era ilegal. “Tuve suerte”, cuenta Mechoulam en una crónica personal del trabajo de su vida, publicada en enero en la revista Annual Review of Pharmacology and Toxicology. “El jefe administrativo de mi instituto conocía a un policía. ... Simplemente fui a la jefatura de policía, me tomé un café con el policía encargado del almacenamiento de drogas ilícitas y conseguí cinco kilos de hachís confiscado, presumiblemente de contrabando desde el Líbano”.
Para 1964, Mechoulam y sus colegas ya habían determinado por primera vez la estructura completa del delta-9-tetrahidrocannabinol, más conocido en todo el mundo como THC (responsable del “subidón” psicoactivo de la marihuana) y del cannabidiol o CBD.
Aquel golpe químico abrió la puerta a la investigación sobre el cannabis. En las décadas siguientes, investigadores como Mechoulam identificaron más de 140 compuestos activos, llamados cannabinoides, en la planta de cannabis, y aprendieron a fabricar muchos de ellos en el laboratorio. Mechoulam ayudó a descubrir que el cuerpo humano produce sus propias versiones naturales de sustancias químicas similares, denominadas endocannabinoides, que pueden influir en nuestro estado de ánimo e incluso en nuestra personalidad. Los científicos han creado cientos de nuevos cannabinoides sintéticos, algunos más potentes que los naturales.
Hoy en día, los investigadores están extrayendo el enorme número de cannabinoides conocidos —antiguos y nuevos, encontrados en plantas o personas, naturales y sintéticos— para posibles usos farmacéuticos. Pero, al mismo tiempo, los cannabinoides sintéticos se han convertido en una tendencia de moda en las drogas recreativas, con efectos potencialmente devastadores.
Los efectos adversos de la mayoría de los cannabinoides sintéticos fabricados hasta ahora superan sus usos médicos, dice el biólogo João Pedro Silva, de la Universidad de Oporto, Portugal, que estudia la toxicología del abuso de sustancias y es coautor de una evaluación de los pros y los contras de estos fármacos publicada en 2023 en la revista Annual Review of Pharmacology and Toxicology. Pero, añade, eso no significa que no haya cosas mejores por venir.
La planta de cannabis produce más de 140 fitocannabinoides; los más conocidos son el cannabidiol (CBD) y el delta-9-tetrahidrocannabinol (THC) (arriba). Estos interactúan con muchos de los mismos receptores que los compuestos producidos por el organismo, llamados endocannabinoides (centro), a pesar de sus diferencias químicas. Los compuestos sintéticos (abajo, se muestran tres) que pretenden imitar la acción de varios cannabinoides también tienen una amplia variedad de estructuras químicas.
La larga historia médica del cannabis
El cannabis se ha utilizado durante siglos por todo tipo de razones, desde calmar la ansiedad o el dolor, hasta estimular el apetito y aliviar las convulsiones. En 2018, se aprobó un medicamento derivado del cannabis —Epidiolex, compuesto de CBD purificado— para controlar las convulsiones en algunos pacientes. Algunas personas con afecciones graves, como esquizofrenia, trastorno obsesivo compulsivo, párkinson y cáncer, se automedican con cannabis en la creencia de que les ayudará, y Mechoulam ve la promesa. “Hay muchos estudios sobre estas enfermedades y los efectos del cannabis (o cannabinoides individuales) en ellas. La mayoría son positivos”, explica a Knowable Magazine.
Esto no quiere decir que el consumo de cannabis no conlleve ningún riesgo. Silva señala que las investigaciones sugieren que los consumidores diarios de cannabis tienen un mayor riesgo de desarrollar trastornos psicóticos, dependiendo de la potencia del cannabis; un trabajo mostró un riesgo entre 3,2 y 5 veces mayor. Los consumidores crónicos a largo plazo pueden desarrollar el síndrome de hiperémesis cannabinoide, caracterizado por vómitos frecuentes. A algunos expertos en salud pública les preocupan los efectos que puede tener a la hora de conducir, y algunas formas recreativas de cannabis contienen contaminantes como metales pesados con efectos desagradables.
Encontrar aplicaciones médicas para los cannabinoides implica comprender su farmacología y sopesar sus pros y sus contras.
Mechoulam tuvo un rol en los inicios de la investigación sobre los posibles usos clínicos del cannabis. Basándose en informes anecdóticos que se remontaban a la antigüedad sobre la ayuda del cannabis en las convulsiones, él y sus colegas estudiaron los efectos del THC y el CBD en la epilepsia. Empezaron con ratones y, como el CBD no mostraba toxicidad ni efectos secundarios, pasaron a las personas. En 1980, entonces en la Universidad Hebrea de Jerusalén, Mechoulam publicó los resultados de un minúsculo ensayo de 4,5 meses con pacientes epilépticos a los que no ayudaban los fármacos actuales. Los resultados parecían prometedores: de las ocho personas que tomaron CBD, cuatro casi no tuvieron ataques a lo largo del estudio y tres experimentaron una mejoría parcial. Solo a un paciente no le ayudó en absoluto.
“Supusimos que estos resultados serían ampliados por las compañías farmacéuticas, pero no ocurrió nada durante más de 30 años”, escribe Mechoulam en su artículo autobiográfico. No fue hasta 2018 cuando la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aprobó el Epidiolex para el tratamiento de ataques epilépticos en personas con ciertas condiciones médicas raras y graves. “Miles de pacientes podrían haber sido ayudados durante las cuatro décadas transcurridas desde nuestra publicación original”, escribe Mechoulam.
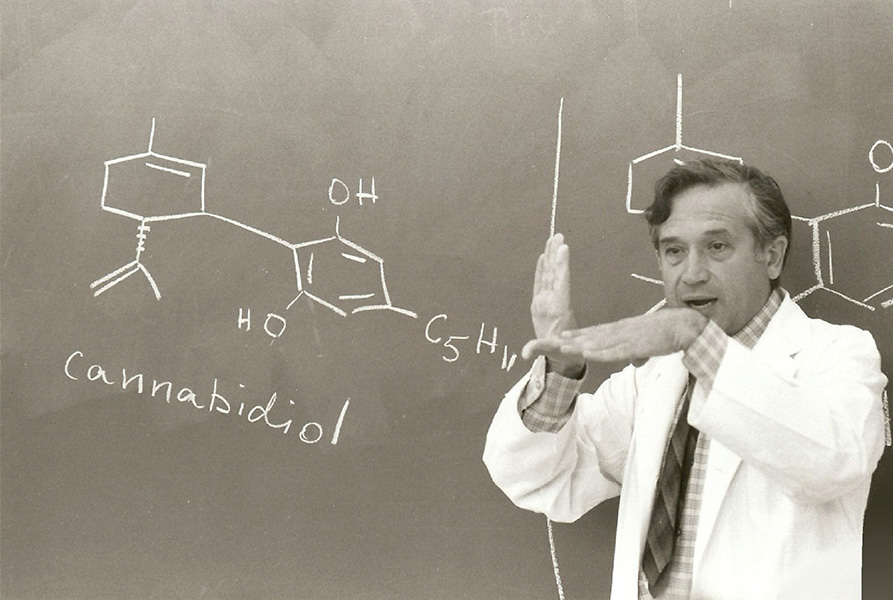
El químico Raphael Mechoulam realizó un trabajo pionero en los años sesenta al descifrar las estructuras químicas de los cannabinoides.
CRÉDITO: R. MECHOULAM / AR PHARMACOLOGY AND TOXICOLOGY 2023
La aprobación de un medicamento es un proceso necesariamente largo, pero en el caso del cannabis se han añadido los obstáculos de las trabas legales, así como la dificultad de obtener protecciones de patentes para los compuestos naturales. Esto último hace que sea difícil para una empresa farmacéutica justificar económicamente los costosos ensayos en humanos y el largo proceso de aprobación ante la FDA.
En la Convención Única de 1961 sobre Estupefacientes de las Naciones Unidas, el cannabis se incluyó en las categorías más restrictivas: Lista I (altamente adictiva y susceptible de abuso) y su subgrupo, Lista IV (con usos medicinales limitados, si es que los tiene). La ONU no retiró el cannabis de la Lista IV hasta diciembre de 2020 y, aunque el cannabis se ha legalizado o despenalizado en varios países y en la mayoría de los estados de EE.UU., sigue estando (polémicamente), tanto en la Lista I de EE.UU. como en la de la ONU, en la misma categoría que la heroína. Se espera que el proyecto de ley estadounidense sobre la investigación del cannabis, aprobado en diciembre de 2022, ayude a aliviar algunos de los problemas que plantea trabajar con cannabis y cannabinoides en el laboratorio.
Hasta la fecha, la FDA solo ha autorizado un puñado de medicamentos basados en cannabinoides, y hasta ahora solo se basan en el THC y el CBD. Junto al Epidiolex, la FDA ha aprobado el THC sintético y un compuesto similar al THC para tratar las náuseas en pacientes sometidos a quimioterapia y la pérdida de peso en pacientes con cáncer o sida. Pero hay indicios de muchos otros posibles usos. El registro de ensayos clínicos de los Institutos Nacionales de la Salud enumera cientos de esfuerzos en marcha en todo el mundo para estudiar el efecto de los cannabinoides en el autismo, el sueño, la enfermedad de Huntington, el tratamiento del dolor y otros.
En los últimos años, dice Mechoulam, el interés se ha extendido más allá del THC y el CBD a otros compuestos del cannabis como el cannabigerol (CBG), que Mechoulam y su colega Yehiel Gaoni descubrieron en 1964. Su equipo ha fabricado derivados del CBG que tienen propiedades antiinflamatorias y analgésicas en ratones (por ejemplo, reducen el dolor que se siente en una pata hinchada) y pueden prevenir la obesidad en ratones alimentados con dietas ricas en grasas. Este año se está realizando un pequeño ensayo clínico sobre los efectos del CBG en el trastorno por déficit de atención con hiperactividad. Mechoulam afirma que la forma de éster metílico de otra sustancia química, el ácido cannabidiólico, también parece “muy prometedora”: en ratas, puede suprimir las náuseas y la ansiedad y actuar como antidepresivo en un modelo animal del trastorno del estado de ánimo.
Pero si la lista de posibles beneficios de todos los cannabinoides es enorme, aún no se ha hecho el trabajo duro para demostrar su utilidad. “Ha sido muy difícil intentar caracterizar los efectos de todos ellos”, afirma Sam Craft, estudiante de doctorado en psicología que estudia los cannabinoides en la Universidad de Bath, en el Reino Unido. “La ciencia aún no se ha puesto al día con todo esto”.
Una versión natural en nuestro cuerpo
Parte de la razón por la que los cannabinoides tienen efectos tan trascendentales es que, como ayudó a descubrir Mechoulam, forman parte de la fisiología humana natural.
En 1988, investigadores dieron a conocer el descubrimiento de un receptor cannabinoide en el cerebro de las ratas, el CB1 (más tarde encontrarían otro, el CB2, y los ubicarían a lo largo de todo el cuerpo humano). Mechoulam pensó que no habría un receptor de este tipo a menos que el cuerpo produjera sustancias químicas similares a los cannabinoides vegetales, así que se puso a buscarlas. Conducía hasta Tel Aviv para comprar cerebros de cerdo que se vendían como alimento, recuerda, y los traía de vuelta al laboratorio. Encontró dos moléculas con actividad similar a la de los cannabinoides: la anandamida (llamada así por la palabra sánscrita ananda, que significa felicidad) y el 2-AG.
Estos endocannabinoides, como se les denomina, pueden alterar nuestro estado de ánimo y afectar a nuestra salud sin que lleguemos a acercarnos a un porro. Algunos especulan que los endocannabinoides pueden ser responsables, en parte, de las peculiaridades de la personalidad, los trastornos de la personalidad o las diferencias de temperamento.
Estudios con animales y células insinúan que la modulación del sistema endocannabinoide podría tener un enorme abanico de posibles aplicaciones, desde la obesidad y la diabetes hasta la neurodegeneración, las enfermedades inflamatorias, los problemas gastrointestinales y cutáneos, el dolor y el cáncer. Algunos estudios han demostrado que los endocannabinoides o creaciones sintéticas similares a los compuestos naturales pueden ayudar a ratones a recuperarse de un traumatismo cerebral, desbloquear arterias en ratas, combatir bacterias resistentes a los antibióticos en placas de Petri y aliviar la adicción a los opiáceos en ratas. Pero el sistema endocannabinoide es complicado y aún no se conoce bien; nadie ha administrado endocannabinoides a personas, lo que para Mechoulam supone un enorme vacío de conocimiento y una gran oportunidad. “Creo que nos estamos perdiendo muchas cosas”, afirma.
“Se trata de un campo de investigación poco explorado”, coincide Silva, y algún día podría dar lugar a fármacos útiles. Por ahora, sin embargo, la mayoría de los ensayos clínicos se centran en comprender el funcionamiento de los endocannabinoides y sus receptores en nuestro cuerpo (incluyendo cómo todo, desde los probióticos al yoga, afecta a los niveles de estas sustancias químicas).
Los receptores cannabinoides CB1 y CB2 se encuentran en todo el cuerpo, desde el cerebro hasta el bazo. Los receptores CB1 son especialmente comunes en el sistema nervioso; los receptores CB2 se concentran en el sistema inmunitario y áreas relacionadas. Pero ambos receptores también están presentes en todo el cuerpo. Esta amplia distribución significa que los compuestos —desde el THC hasta los endocannabinoides y los cannabinoides sintéticos— que se unen a uno de estos receptores o a ambos pueden afectar a una gran variedad de sistemas, como la percepción del dolor, la actividad motora, el apetito y la memoria a corto plazo.
‘Efectos tóxicos’ de los productos sintéticos
Tras el descubrimiento de los CB1 y CB2, muchos investigadores se centraron en diseñar nuevas moléculas sintéticas que se unieran a estos receptores con más fuerza que los cannabinoides vegetales. Las empresas farmacéuticas llevan décadas buscando estos cannabinoides sintéticos, pero hasta ahora, según Craft, sin mucho éxito y con algunos errores. Un fármaco llamado Rimonabant, que se unía fuertemente al receptor CB1 pero actuaba en oposición al efecto habitual del CB1, fue aprobado en Europa y otros países (pero no en EE.UU.) a principios de la década de 2000 para ayudar a disminuir el apetito y combatir así la obesidad. Fue retirado en todo el mundo en 2008 debido a sus graves efectos secundarios psicóticos, entre ellos provocar depresión y pensamientos suicidas.
Algunos de los productos sintéticos inventados originalmente por académicos y empresas farmacéuticas han acabado en drogas recreativas como Spice y K2. Estas drogas están en auge y siguen apareciendo nuevas formulaciones químicas: desde 2008, se han detectado 224 diferentes en Europa. Estos compuestos, modificados químicamente para maximizar los efectos psicoactivos, pueden causar desde dolores de cabeza y paranoia, hasta palpitaciones, insuficiencia hepática y muerte. “Tienen efectos muy tóxicos”, afirma Craft.
Por ahora, dice Silva, hay escasas pruebas de que los cannabinoides sintéticos existentes sean útiles desde el punto de vista medicinal: a medida que la mayoría de los candidatos a fármacos se han ido desarrollando, han tendido a aparecer efectos adversos. Por ello, la mayoría de los esfuerzos farmacéuticos por desarrollar cannabinoides sintéticos se han interrumpido.
Pero eso no significa que toda la investigación se haya detenido; un cannabinoide sintético llamado JWH-133, por ejemplo, se está investigando en roedores por su potencial para reducir el tamaño de los tumores de cáncer de mama. Es posible hacer decenas de miles de modificaciones químicas distintas de los cannabinoides, por lo que, dice Silva, “es probable que algunas de estas combinaciones puedan tener potencial terapéutico”. El sistema endocannabinoide es tan importante en el cuerpo humano que hay mucho margen para explorar todo tipo de ángulos medicinales. Por ejemplo, Mechoulam forma parte del consejo asesor de la empresa EPM, con sede en Israel, cuyo objetivo específico es desarrollar medicamentos basados en versiones sintéticas de unos tipos de compuestos cannabinoides llamados ácidos cannabinoides sintéticos.
Con todo este trabajo en marcha sobre la química de estos compuestos y su funcionamiento dentro del cuerpo humano, Mechoulam, que ahora tiene 92 años, ve una próxima explosión en la comprensión de la fisiología del sistema endocannabinoide. Y con ello, dice, “supongo que tendremos muchos fármacos nuevos”.
Artículo traducido por Debbie Ponchner
10.1146/knowable-031723-1
Apoye a la revista Knowable
Ayúdenos a hacer que el conocimiento científico sea accesible para todos
DONAREXPLORE MÁS | Lea artículos científicos relacionados