Sus células están muriendo… todo el tiempo
Algunas se desvanecen en calma. Otras mueren de forma menos bonitas en accidentes extraños o invasiones mortales, o después de una exhibición ostentosa.
Manténgase informado
Suscríbase al boletín de noticias de Knowable en español
Miles de millones de células mueren en nuestro cuerpo cada día. Algunas lo hacen de manera más notoria, otras se van en silencio.
Pueden morir por un accidente si sufren una lesión o una infección. Por otra parte, si superan su expectativa de vida natural o comienzan a fallar, pueden organizar una meticulosa desaparición deseable, con sus restos ordenados de manera cuidadosa.
Al principio, los científicos pensaban que esas eran las únicas dos formas en que una célula animal podía morir: por accidente o de esa manera limpia y ordenada. Pero en las últimas dos décadas, los investigadores han acumulado muchos más escenarios novedosos de muerte celular, algunos específicos para ciertos tipos de células o situaciones. Comprender esta panoplia de formas de morir podría ayudar a los científicos a salvar células buenas y matar a las malas, lo que conduciría a tratamientos para infecciones, enfermedades autoinmunitarias y cáncer.
“Hay muchos, muchos sabores diferentes”, dice Michael Overholtzer, biólogo celular del Memorial Sloan Kettering Cancer Center de Nueva York. Calcula que ahora hay más de 20 nombres para describir las variedades de muerte celular.
Aquí, Knowable Magazine describe algunas de las maneras clásicas y otras nuevas por las que las células pueden morir.
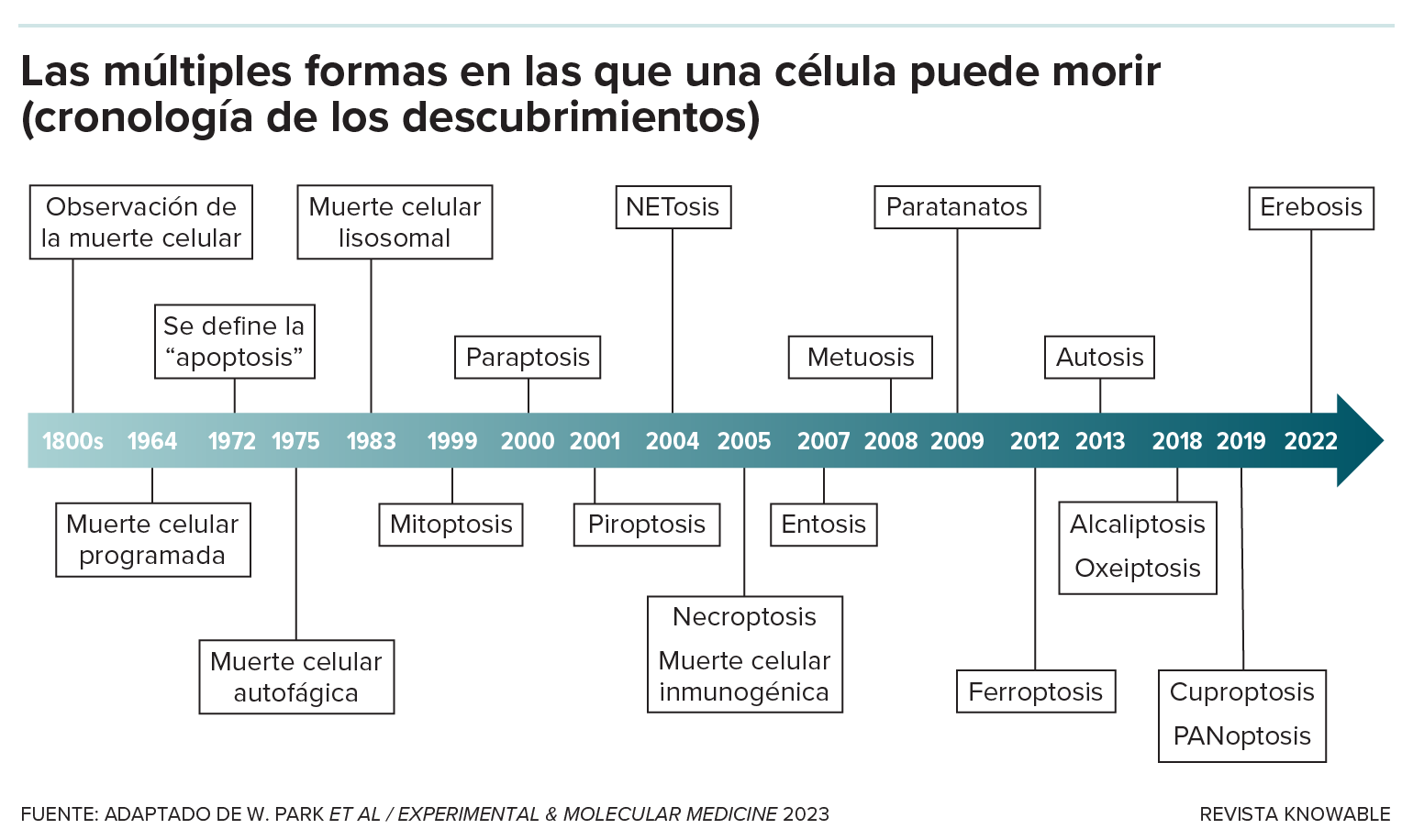
La identificación de nuevas formas de muerte celular se ha acelerado en los últimos años.
Muerte celular no planificada: necrosis
A las células les pueden pasar muchas cosas malas: se lastiman o se queman, se envenenan o se les priva de oxígeno, se infectan con microbios o enferman de alguna otra manera. Necrosis es el nombre que se le da cuando una célula muere por accidente.
Existen varios tipos de necrosis, ninguno de ellos agradable: en el caso de la gangrena, cuando las células se ven privadas de sangre, se pudren. En otros casos, las células moribundas se licúan y a veces se convierten en una sustancia viscosa amarilla. Las células pulmonares dañadas por la tuberculosis se vuelven blandas y blancas —“caseosa”, el nombre técnico para este tipo de necrosis, literalmente significa “parecida al queso”—.
Cualquier forma de muerte que no sea la necrosis se considera “programada”, lo que significa que la célula la lleva a cabo de manera intencional porque está dañada o ha dejado de ser útil.
Una buena y ordenada muerte: la apoptosis
Las dos categorías principales de muerte celular programada son “silenciosa y violenta”, dice Thirumala-Devi Kanneganti, inmunóloga del St. Jude Children’s Research Hospital en Memphis, Tennessee. La apoptosis, descrita por primera vez en 1972, es el tipo silencioso original: es una forma limpia y ordenada de muerte celular que no despierta al sistema inmunitario.
Eso es útil cuando las células están dañadas o han cumplido su propósito. La apoptosis permite a los renacuajos deshacerse de las células de la cola cuando se convierten en ranas, por ejemplo, o a los embriones humanos, deshacerse de la membrana entre los dedos en desarrollo.
La célula se encoge y se separa de sus vecinas. El material genético en el núcleo se rompe en pedazos que se estrujan, y el núcleo se fragmenta. La membrana se abulta y se ampolla, y la célula se desintegra. Otras células devoran los pedazos, manteniendo el tejido ordenado.
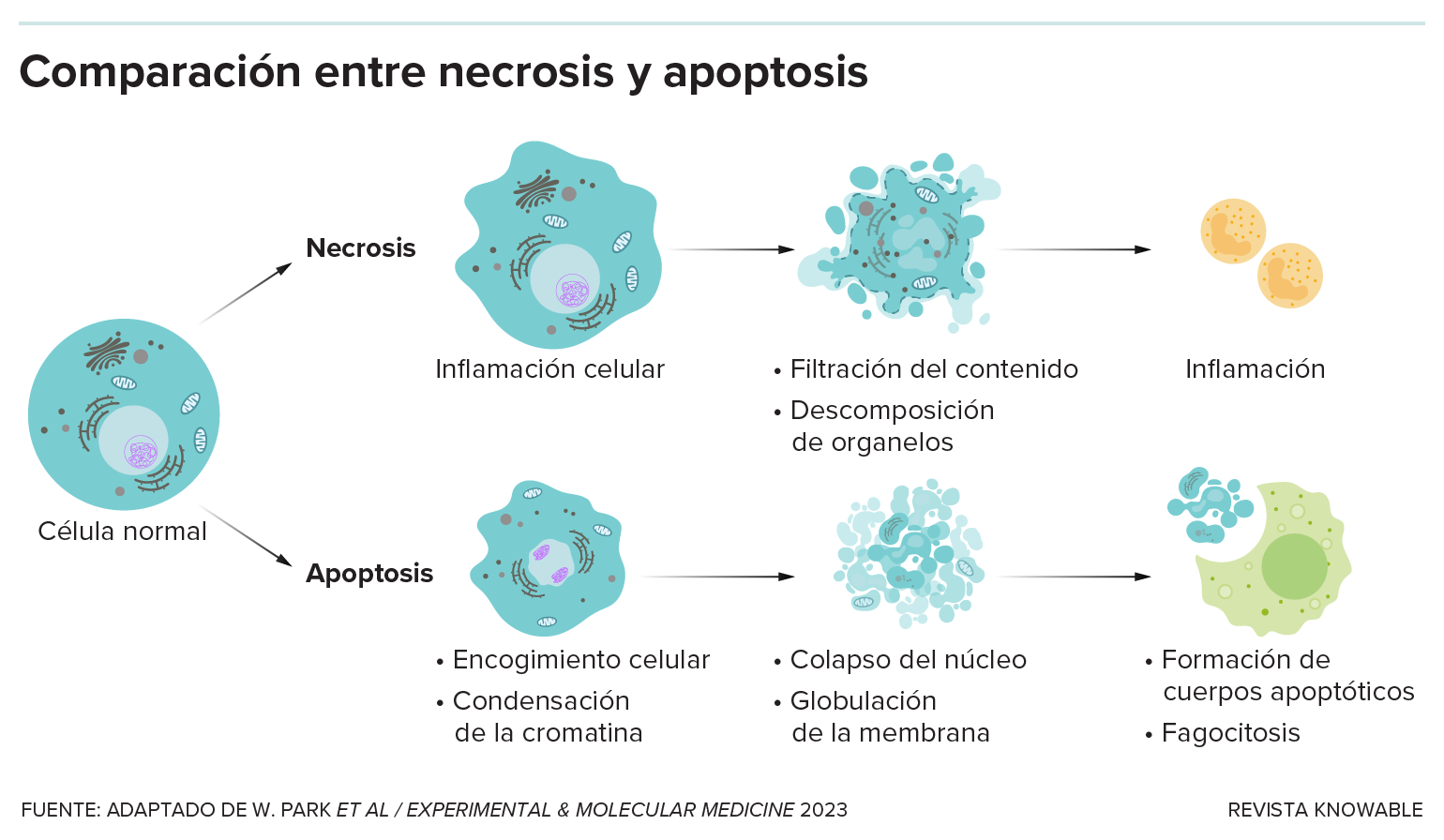
En la necrosis, una célula muere por accidente, libera su contenido y atrae a las células inmunitarias al lugar del daño, creando una inflamación. En la apoptosis, la célula colapsa sobre sí misma y los fragmentos se eliminan sin causar una inflamación perjudicial.
Banderas rojas: necroptosis y piroptosis
Se trata de las formas violentas de muerte celular, y ayudaron a ampliar el repertorio más allá de la apoptosis y la necrosis. Suelen activarse cuando las células han sido secuestradas por virus u otros agentes infecciosos. En lugar de reducirse a fábricas de virus, se suicidan. Estas células mueren agitando grandes banderas rojas en forma de sustancias químicas que liberan para alertar al sistema inmunitario para que se active y salve a sus vecinas.
En un estudio de 1998, un equipo inhibió la capacidad activar la apoptosis en células cultivadas en placas de laboratorio, y las células murieron de todos modos. Pero lo hicieron de una manera desordenada que se llamó necroptosis por su mezcla de características de la apoptosis y la necrosis. Al igual que con la necrosis, las células y sus organelos se inflaman y luego la membrana externa se rompe. La necroptosis es un mecanismo de respaldo útil porque algunos agentes infecciosos pueden desactivar la apoptosis.
Luego está la piroptosis, observada por primera vez en 1992 en glóbulos blancos infectados con la bacteria de la disentería y bautizada en 2001. Se trata de “la muerte proinflamatoria, estridente y alarmante de una célula potencialmente peligrosa”, escribieron quienes le dieron el nombre. Al igual que con la necroptosis, las células se inflaman. Luego, activan enzimas que perforan la membrana celular, de modo que su contenido se filtra y provoca una respuesta inmunitaria.
Ya sea por piroptosis o necroptosis, esa respuesta inmunitaria es necesaria para activar las defensas del cuerpo contra las infecciones, como la fiebre que achicharra a los invasores, dice Kanneganti, coautor de un artículo sobre las moléculas involucradas en la muerte celular publicado en el Annual Review of Immunology de 2020. Pero si mueren demasiadas células o el sistema inmunitario se queda atascado en la posición de “encendido”, eso puede provocar una inflamación continua o una enfermedad autoinmune.
Mezclar y combinar: PANoptosis
Las células inmunitarias también pueden necesitar morir en caso de infección, inflamación o incluso cáncer. Cuando el grupo de Kanneganti investigaba este proceso notaron un modo alternativo de muerte que incorporaba elementos de apoptosis, necroptosis y piroptosis. Utilizando la primera letra de cada tipo clásico lo llamaron PANoptosis. Desde entonces, los investigadores han encontrado este método híbrido de muerte también en otros tipos de células.
En la PANoptosis, la célula ensambla una gran máquina de proteínas llamada PANoptosoma. Esto activa enzimas para perforar las membranas de la célula. A medida que muere, la célula libera moléculas de alerta que le dicen a otras células inmunitarias que hay un problema.
¿Por qué las células necesitan tantas formas de lograr el mismo fin fatal? Las células probablemente desarrollaron estas diferentes opciones durante una carrera armamentista contra microbios causantes de enfermedades, presume Kanneganti. Los microbios, con el objetivo de sobrevivir, pueden tratar de desactivar la muerte celular. Pero si la célula tiene un amplio menú de mecanismos de muerte puede suicidarse de otra manera, sacrificándose para obstaculizar al patógeno.
Muerte kamikaze: NETosis
Las células inmunitarias pueden sacrificarse de manera aún más dramática, en una acción kamikaze que también elimina a los patógenos circundantes. Este acto sensacional es competencia de los glóbulos blancos llamados neutrófilos, que patrullan las áreas de infección y se tragan a los invasores.
Pero a veces, los agentes infecciosos son demasiado grandes o demasiado numerosos para devorarlos. Los neutrófilos cambian de táctica y vomitan su propio ADN sobre el patógeno, atrapando a los invasores en una especie de red genómica. Se llama NETosis (NET por “trampas extracelulares de neutrófilos”, en inglés). Luego, otras células eliminan los patógenos enredados.
En ocasiones, la célula que lanza la red ya está muriendo o muere mientras esto sucede, lo que la convierte en una célula zombi que comete un último acto altruista, dice el inmunólogo Ben Croker, que estudia el fenómeno en la Facultad de Medicina de la Universidad de California, en San Diego
Muerte metálica: cuproptosis y ferroptosis
Si bien las células cancerosas parecen amenazadoras, en realidad son bastante vulnerables a la muerte, dice Todd Golub, biólogo del cáncer del Instituto Broad en Cambridge, Massachusetts. “La clave”, agrega, “es encontrar los desencadenantes adecuados”.
El grupo de Golub halló un desencadenante en medicamentos que transportan cobre a las células. El equipo todavía está buscando entender cómo eso hace que las células mueran en un proceso que, en 2022, bautizaron como cuproptosis.
El hierro también puede ser mortal para las células cancerosas, como descubrió el biólogo químico Brent Stockwell, de la Universidad de Columbia en Nueva York. Además de los tumores, las células normales del cerebro, el hígado y los riñones parecen ser particularmente susceptibles a esta forma de muerte celular, a la que en 2012 denominó ferroptosis. Los investigadores también han observado ferroptosis en una amplia gama de organismos, incluso levaduras y plantas, dice Stockwell, quien coescribió una descripción sobre las características clave de la ferroptosis en el Annual Review of Cancer Biology de 2019.
Stockwell y otros investigadores están trabajando para identificar fármacos o dietas especiales que podrían activar la ferroptosis para combatir el cáncer o bloquearla para proteger a las células de morir en enfermedades como el alzhéimer.
Cómeme: entosis
Overholtzer notó algo extraño mientras estudiaba células de cáncer de mama a principios de los años 2000: había células cancerosas que se introducían en otras células. En 2007, él y su supervisor de laboratorio denominaron entosis a este fenómeno.
La célula invasora termina encerrada en una gran burbuja membranosa. Puede morir de hambre y sufrir apoptosis, o ser asesinada por la célula circundante. Luego, la célula exterior digiere sus restos.
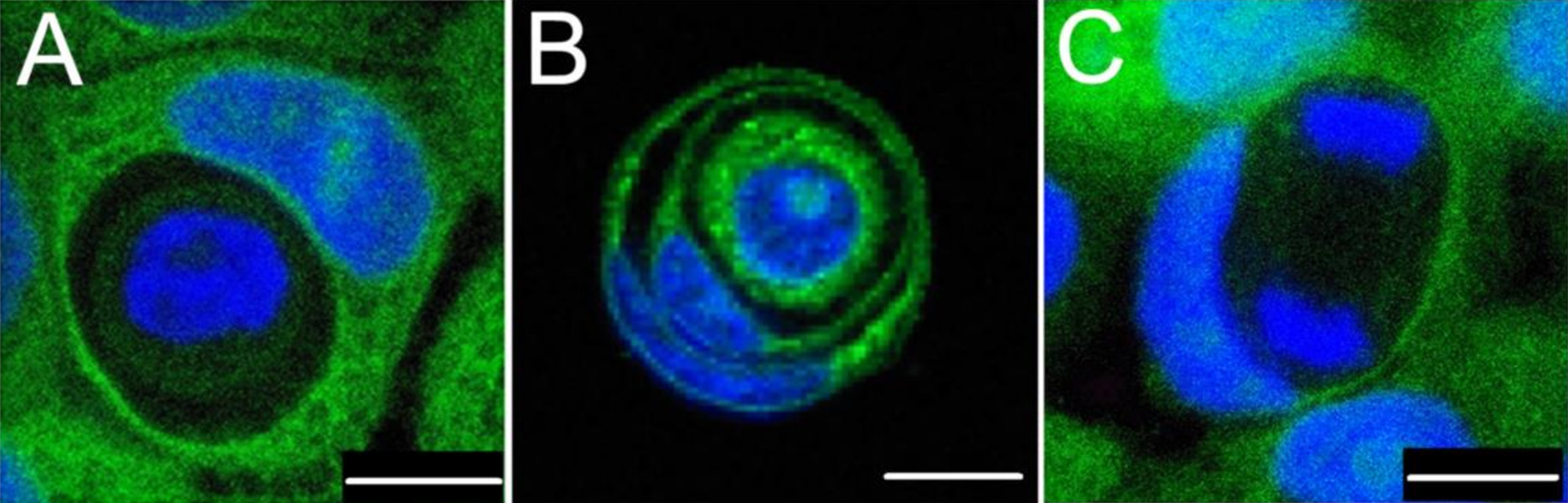
Durante la entosis, una célula se inserta dentro de otra. En estas imágenes, el azul indica el ADN celular y el verde el citoplasma. Una célula puede existir dentro de otra célula (A); una célula puede existir dentro de una célula que está dentro de otra célula (B); y una célula interna puede dividir su ADN (C).
CRÉDITO: I. MLYNARCZUK-BIALY ET AL / CANCERS 2020
Pero a veces, extrañamente, sobrevive y sale de la célula para vivir de nuevo de forma independiente. Al notar esto, algunos científicos han propuesto que la entosis ofrece a las células cancerosas una manera de esconderse temporalmente del sistema inmunitario o de los medicamentos contra el cáncer.
Aún hay mucho que aprender sobre las muertes celulares, y es probable que haya modos de muerte que todavía esperan ser descubiertos, especula Golub.
En última instancia, el estudio de la vida requiere la investigación de la muerte celular. Como escribió el autor japonés Haruki Murakami: “La muerte existe, no como lo opuesto a la vida, sino como parte de ella”.
Artículo traducido por Daniela Hirschfeld
10.1146/knowable-110524-1
Apoye a la revista Knowable
Ayúdenos a hacer que el conocimiento científico sea accesible para todos
DONAREXPLORE MÁS | Lea artículos científicos relacionados