Órganos de cerdo en humanos: el futuro de los trasplantes entre especies
¿Pueden los animales modificados genéticamente ayudar a solucionar la escasez de órganos para trasplantes? Luego de años de investigación sobre los xenotrasplantes, el campo se encuentra en un punto de inflexión —pero aún existen riesgos y dilemas éticos—.
Manténgase informado
Suscríbase al boletín de noticias de Knowable en español
Más de 100.000 personas en Estados Unidos esperan un nuevo corazón, un riñón o algún otro órgano. Muchas morirán mientras esperan. Algunos científicos ven una nueva esperanza para estas personas en los órganos de cerdos que han sido modificados genéticamente para funcionar dentro del cuerpo humano.
Estos trasplantes entre especies, llamados xenotrasplantes, ofrecen una solución técnica para un problema básico: hay más personas que necesitan un órgano que órganos disponibles, ya sean de donantes vivos o con muerte cerebral.
“Desafortunadamente, mientras hablamos, alguien está muriendo esperando un órgano”, dice el cirujano Muhammad Mansoor Mohiuddin, director del programa de xenotrasplante cardíaco de la Universidad de Maryland, en Baltimore.
En los últimos años, un puñado de personas en Estados Unidos y China han recibido riñones, corazones e hígados de cerdo especialmente modificados, pero lograr que esos órganos funcionen de manera segura en una persona es un gran desafío, como se describe en el Annual Review of Animal Biosciences de 2024. Ahora, gracias a los avances tecnológicos y médicos, la compañía United Therapeutics, en Silver Spring, Maryland, está iniciando los primeros ensayos clínicos oficiales de xenotrasplantes, y muchos investigadores creen que el procedimiento podría convertirse en una práctica de rutina.
Sin embargo, hay preguntas que persisten, incluidos los riesgos de que los órganos de cerdo transmitan virus a las personas, y una serie de preocupaciones éticas. Aquí presentamos un vistazo a la situación actual y lo que puede estar por venir.
Combatir el rechazo
Después de una larga historia de experimentos con trasplantes de animales, los científicos se han enfocado en los cerdos, o minicerdos, como fuente de órganos. Estos animales se reproducen y crecen rápidamente, sus órganos tienen aproximadamente el tamaño adecuado y no hay muchos patógenos que infecten tanto a los cerdos como a las personas.
“Creo que un cerdo es casi un donante ideal para el trasplante en humanos”, dice Wenning Qin, vicepresidente sénior de innovación en eGenesis, una empresa con sede en Cambridge, Massachusetts, que diseña minicerdos como fuente de órganos.
Pero si no se hacen ajustes especiales a esos órganos, el cuerpo humano los atacará de inmediato. Este “rechazo hiperagudo” se desencadena cuando los anticuerpos humanos reconocen como extrañas moléculas de tres azúcares en los vasos sanguíneos de un órgano de cerdo. Los anticuerpos se adhieren a las células y dan inicio a una cadena de eventos que coagula la sangre, bloqueando su flujo. “En 10 minutos, el órgano puede pasar de un color rosado a negro”, dice Qin. “El órgano está muerto”.
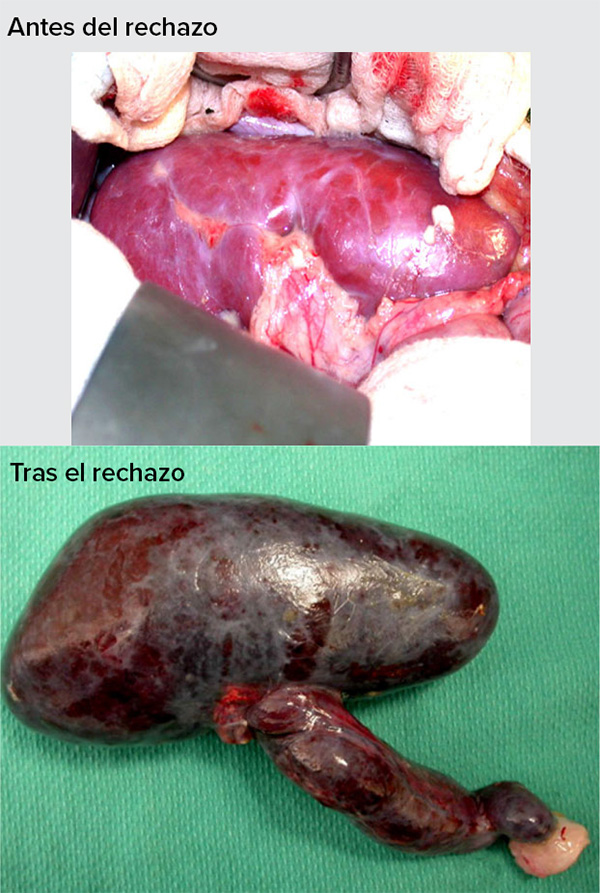
En un proceso llamado rechazo hiperagudo, los anticuerpos del receptor reconocen un órgano como extraño y lo atacan de inmediato: el flujo sanguíneo se bloquea y mata rápidamente al órgano. Los órganos de cerdo utilizados en trasplantes han sido diseñados para evitar este tipo de rechazo.
CRÉDITO: D.K.C. COOPER ET AL / XENOTRANSPLANTATION 2016
Para resolver el problema del rechazo hiperagudo, empresas como eGenesis y United Therapeutics han utilizado el sistema de edición genética basado en CRISPR/Cas para modificar el ADN porcino. Por ejemplo, eGenesis destruyó los tres genes responsables de la producción de esos azúcares problemáticos de los cerdos. Pero el sistema inmunitario humano todavía tiene formas de reconocer y rechazar el órgano extraño —solo que más tarde—. Y los fármacos inmunosupresores estándar, diseñados para trasplantes de humano a humano, no pueden prevenir por completo esa respuesta al xenotrasplante, dice Mohiuddin.
Para ayudar a enfrentar ese rechazo en una etapa posterior, ambas empresas también agregaron varios genes humanos a las células de cerdo. Estos genes producen proteínas que se ubican en la superficie celular, disfrazando a las células de cerdo como humanas. En 2023, eGenesis reportó que cinco de los 15 monos macacos cangrejeros que recibieron riñones de cerdos de la empresa sobrevivieron durante más de un año.
Y para frenar aún más esa respuesta en una etapa posterior, Mohiuddin y otros han desarrollado fármacos que suprimen aún más las respuestas de las células inmunitarias. En experimentos con corazones de cerdo trasplantados en el abdomen de cinco babuinos, ese tratamiento permitió que los corazones trasplantados sobrevivieran hasta dos años y medio.
Otros investigadores esperan eliminar la necesidad de fármacos a largo plazo entrenando al sistema inmunitario del receptor del órgano para que ignore los tejidos trasplantados, ya sean de humanos u otra especie. Megan Sykes, directora del Centro de Inmunología Traslacional de la Universidad de Columbia en Nueva York, está abordando este problema trasplantando tejido adicional del sistema inmunitario del donante —ya sea células de la médula ósea o del timo— al receptor. Se espera que este enfoque haga que el sistema inmunitario del receptor sea más tolerante a los tejidos del donante. Actualmente, está probando si puede retirar de forma segura los medicamentos inmunosupresores de los babuinos que recibieron órganos de cerdo más tejido de timo. (Sykes ha recibido financiación para su investigación de United Therapeutics).
Sykes dice que “es un momento emocionante” para el campo de los xenotrasplantes. “Creo que vamos a ver algunos avances significativos en los pacientes en el futuro cercano”.
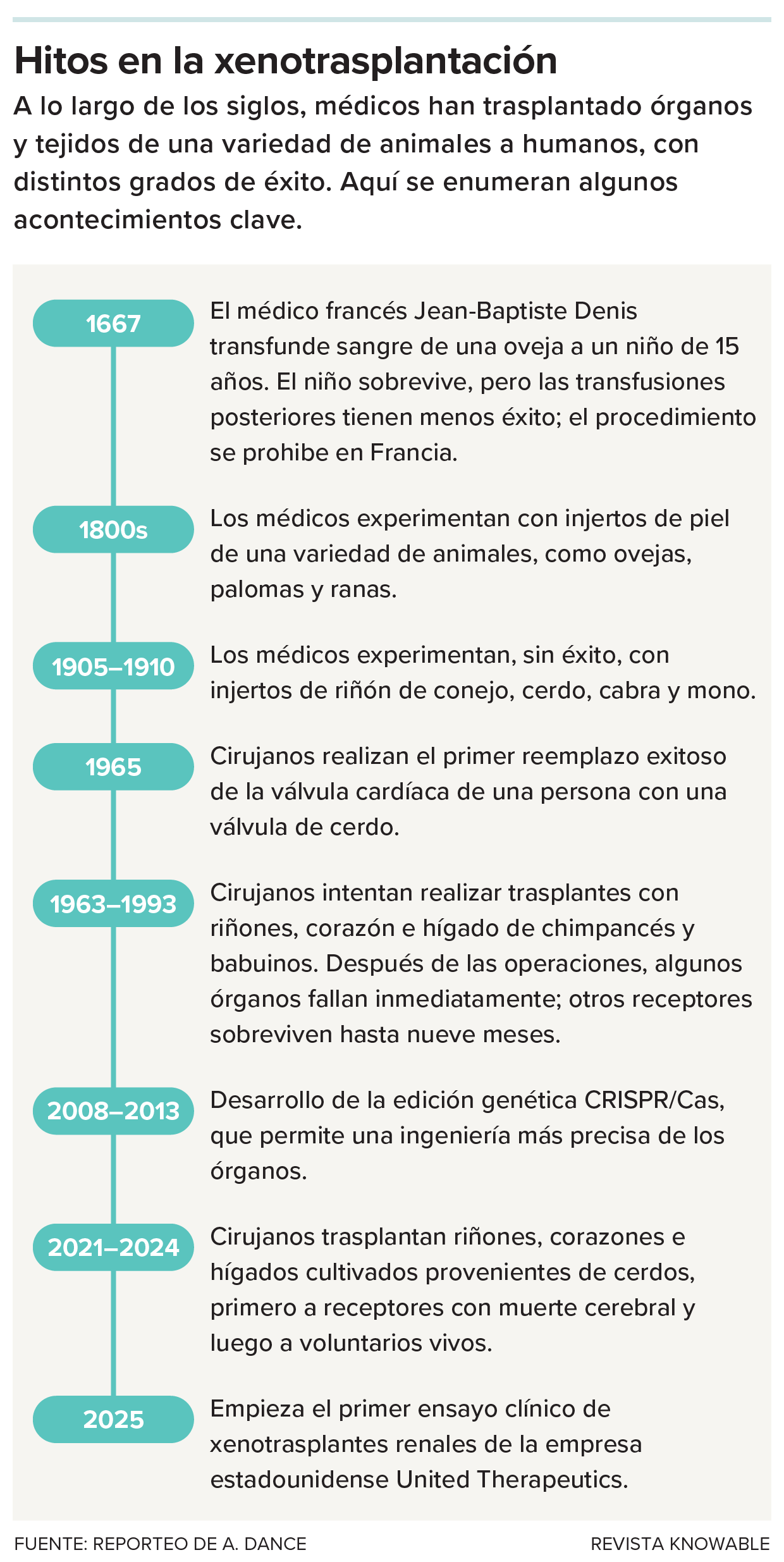
Aquí algunos momentos clave en la historia de los trasplantes entre especies.
Preocupaciones éticas
Hasta ahora se han realizado más de una docena de trasplantes de órganos de cerdos en humanos. Los primeros trasplantes fueron experimentos de corta duración en pacientes con muerte cerebral, por lo que no había ningún riesgo adicional para la salud humana. En un puñado de estos casos, los investigadores informaron que los corazones de cerdos modificados genéticamente podían latir, los hígados producían bilis y los riñones podían funcionar, produciendo orina, sin rechazo inmediato.
Luego, los cirujanos pasaron a los receptores vivos. Estos voluntarios estaban demasiado enfermos o no eran aptos para un trasplante de órgano humano.
Algunos expertos en ética han expresado su preocupación por la forma en que se selecciona a estos pacientes humanos. En estos primeros trasplantes, los médicos se acercaron a los receptores elegibles y solicitaron la aprobación de la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) por la vía de “uso compasivo”, que permite que una persona gravemente enferma reciba un tratamiento no aprobado o no probado.
“Son pacientes a los que se les está haciendo una oferta que no pueden rechazar”, dice L. Syd Johnson, bioeticista de la SUNY Upstate Medical University, en Syracuse. Es posible que esperen mucho más de lo que se les promete, añade Johnson: “No creo que las personas se estén sometiendo a una cirugía mayor ni a inmunosupresión y a todos los diversos riesgos que conllevan, para sobrevivir tres días, tres semanas o seis semanas”.
Mohiuddin, que afirma que la comunidad científica está “totalmente en deuda” con estos pacientes, agrega que los receptores son muy conscientes de los riesgos de estos procedimientos experimentales. Las primeras cuatro personas que recibieron riñones o corazones de cerdo murieron en cuestión de semanas o meses, pero el experto asegura que los médicos y los científicos aprendieron lecciones valiosas —por ejemplo, que es importante iniciar la inmunosupresión antes de que se realice el trasplante—.
Estos hallazgos ayudaron a que los trasplantes posteriores fueran mejores; una mujer de Alabama, que recibió un riñón de cerdo en el Instituto de Trasplantes Langone de la Universidad de Nueva York en noviembre de 2024, recibió autorización para regresar a su casa a fines de febrero.
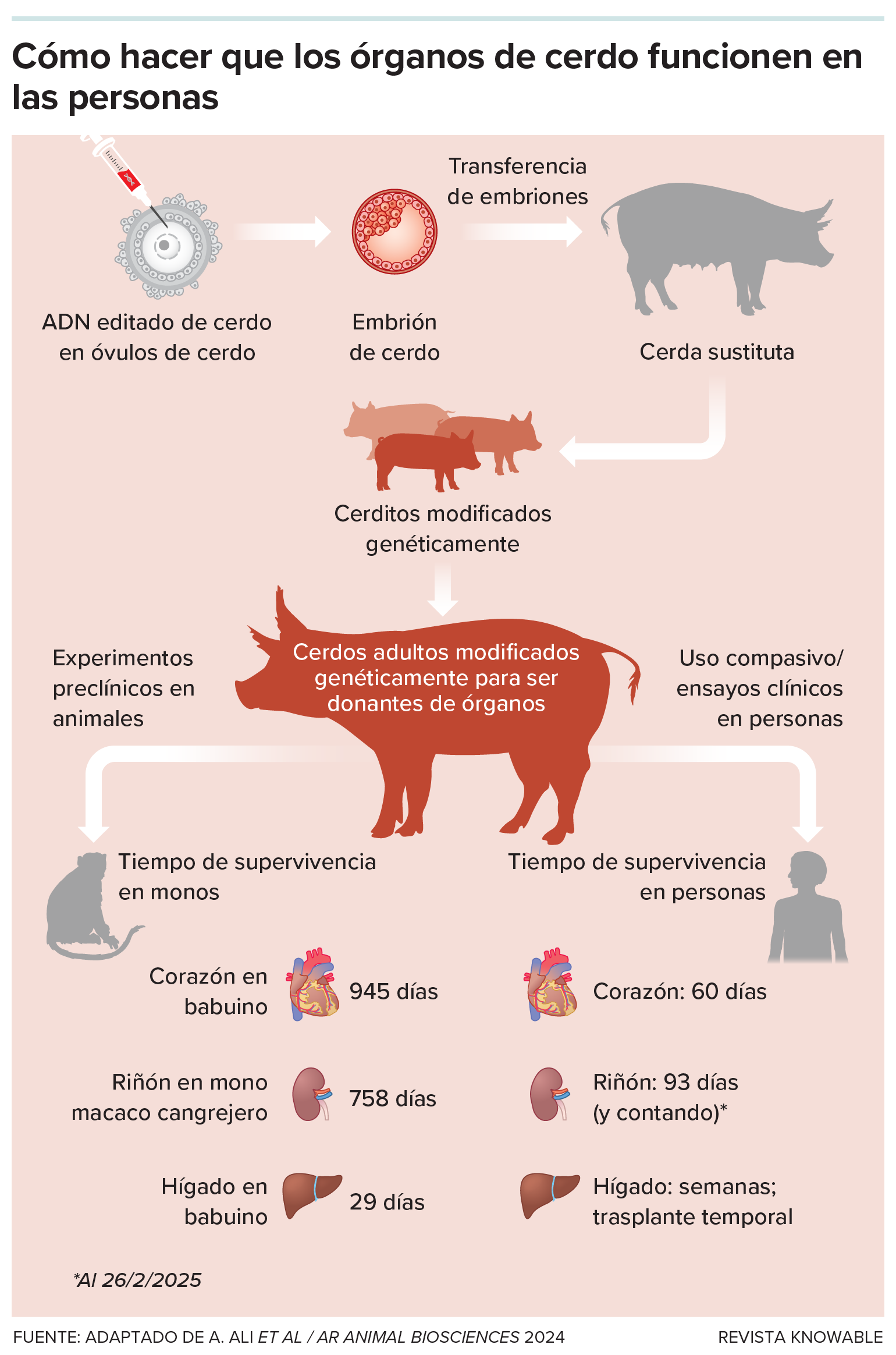
Para producir órganos que el cuerpo humano no rechace, los científicos editan el ADN de cerdo, lo transfieren a un óvulo y crían cerditos modificados. Esos órganos han durado semanas o años en trasplantes experimentales en monos y, hasta ahora, meses en personas.
La preocupación por la propagación de virus
Los científicos también están preocupados porque los cerdos que son portadores de virus podrían infectar a los receptores humanos de trasplantes, o incluso a las personas con las que interactúan esos pacientes. Son de especial preocupación los llamados retrovirus endógenos porcinos que se esconden en el genoma del cerdo. Una vez más, la edición genética CRISPR/Cas ofreció una solución: eGenesis hizo ediciones adicionales en sus animales; 59 de los 69 cambios fueron para destruir esos retrovirus.
Un virus porcino diferente fue detectado en David Bennett, que recibió un trasplante: en 2022, fue el primero en recibir un corazón de cerdo de la empresa United Therapeutics, con 10 modificaciones genéticas. Las pruebas realizadas luego del trasplante detectaron en su sangre ADN de un citomegalovirus porcino. El virus probablemente estaba inactivo y no infectó ninguna de las células de Bennett, dice Mohiuddin, quien codirigió el equipo del trasplante. El paciente murió después de dos meses debido a una insuficiencia cardíaca que, según Mohiuddin, probablemente fue resultado del rechazo al órgano. Ahora hay disponibles pruebas de virus más sensibles, detalla Mohiuddin.
Incluso un pequeño riesgo de transmisión viral tiene amplias implicaciones para las personas, porque virus graves e incluso pandémicos como el VIH y probablemente el virus de la Covid-19 han surgido cuando virus de otros animales llegaron a los humanos. Los virus que pasan de una especie a otra pueden evolucionar y volverse más agresivos, en especial en personas con sistemas inmunitarios debilitados —como los enfermos que toman inmunosupresores—.
Por ello, el Servicio de Salud Pública de Estados Unidos y la Asociación Internacional de Xenotrasplantes han recomendado que los pacientes que reciben xenotrasplantes sean monitoreados durante toda la vida. Pero eso significa que los pacientes no tienen el derecho habitual de quienes participan en un ensayo a retirarse de un estudio en cualquier momento, dice Johnson. El monitoreo podría extenderse a las personas con las que interactúan, que nunca dieron su consentimiento para participar en un estudio.
Otra forma de protegerse contra los virus es mantener a los cerdos en entornos estériles —pero puede que los animales no estén tan dispuestos—. Los cerdos son animales inteligentes y sociales, y realmente les gusta revolcarse en el barro; las condiciones estériles de laboratorio probablemente les provoquen “daños psicológicos y sociales”, dice Johnson. Aunque el mundo sacrifica casi 1.500 millones de cerdos cada año que se destinan como alimento, agrega que eso no significa necesariamente que sea ético crear más animales para uso médico.
¿Quién se beneficia y quién paga?
Si los xenotrasplantes se convierten en una práctica médica habitual surge otro embrollo ético: ¿cómo se distribuirán esos órganos y quién pagará por ellos? Los dos primeros trasplantes en la Universidad de Maryland costaron alrededor de 1,5 millones de dólares cada uno, dice Mohiuddin; uno fue cubierto por la universidad y el otro por el patrocinador del estudio, United Therapeutics.
“Preferiría que dedicáramos nuestro tiempo y recursos a otras cosas, a prevenir el fallo de órganos, a tratarlo, a regenerarlos”, opina Johnson.
Sin embargo, los defensores de los xenotrasplantes están ansiosos por comenzar los ensayos clínicos. La FDA ha autorizado a eGenesis y a sus colaboradores a realizar tres trasplantes de riñón por uso compasivo. La primera operación, en un hombre de New Hampshire, se realizó el 25 de enero y el paciente ha sido dado de alta del hospital. Mientras tanto, United Therapeutics ha obtenido el visto bueno de la FDA para un ensayo clínico en pacientes renales, que comenzará a mediados de 2025 con seis pacientes, y podría llegar a incluir a 50 receptores.
“No estamos afirmando que ya tengamos una solución perfecta”, dice Mohiuddin, pero espera que, con el tiempo, los xenotrasplantes puedan convertirse en un complemento válido al suministro de órganos humanos. Las ediciones adicionales en los órganos de cerdo o el progreso médico vinculado a la tolerancia podrían hacer innecesaria la inmunosupresión a largo plazo.
“No habrá escasez de órganos si se llega a esa etapa”, afirma Mohiuddin.
Artículo traducido por Daniela Hirschfeld
10.1146/knowable-032525-1
Apoye a la revista Knowable
Ayúdenos a hacer que el conocimiento científico sea accesible para todos
DONAREXPLORE MÁS | Lea artículos científicos relacionados