En los albores de la vida, ¿se originó primero el metabolismo?
Algunos científicos proponen que, al principio, la geoquímica dio paso a la bioquímica, sin necesidad de material genético. Fue solo más tarde cuando aparecieron el ARN y el ADN.
Manténgase informado
Suscríbase al boletín de noticias de Knowable en español
Hace cuatro mil millones de años, nuestro planeta era agua y roca estéril. De esto, surgió una química muy complicada, tal vez en un estanque o en una profunda chimenea submarina. Con el tiempo, esa química se envolvió en membranas, se desarrolló una célula primitiva y la vida surgió del limo.
Pero, ¿cómo? Entre los muchos misterios, hay un problema del huevo o la gallina por resolver. Las proteínas denominadas enzimas, que ponen en marcha reacciones químicas dentro de las células, se crean a partir de instrucciones contenidas en el material genético: el ADN o el ARN. Pero al principio, esas moléculas no existían: para fabricarlas, se necesitan enzimas.
Entonces, ¿qué puso las cosas en marcha?
Una idea que los científicos han barajado durante mucho tiempo es que el material genético fue lo primero —en forma de una molécula llamada ARN, un primo cercano del ADN—. La belleza del ARN es su versatilidad: puede catalizar reacciones químicas y también almacenar información genética. Así que tal vez en un lago en la superficie de la Tierra, las moléculas se concentraron por evaporación y luego se unieron para formar las primeras cadenas de ARN.
Pero hasta ahora, los científicos no han sido capaces de crear moléculas de ARN en experimentos que imiten las sopas de sustancias químicas simples que habrían existido en la Tierra primitiva. “Ha habido informes de cómo hacerlo, pero siempre parecen un poco artificiales”, dice Albert Fahrenbach, químico orgánico de la Universidad de Nueva Gales del Sur en Sídney —aunque añade que los defensores dicen que tal dificultad es solo de esperar—.
Es difícil imaginar que un sistema de cadenas de ARN autorreplicantes pudiera haberse organizado espontáneamente, dice Robert Pascal, un químico que trabaja en los orígenes y el surgimiento de la vida en la Universidad de Aix-Marsella en Francia. “Creo que, en realidad, nadie cree ahora que pudiera haber sido posible”.
Otra posibilidad es que la bioquímica fuera lo primero —evolucionó como geoquímica, fuera de las células—. Las reacciones químicas habrían tenido lugar sin enzimas al principio, muy lentamente. Las reacciones avanzarían poco a poco porque estaban favorecidas termodinámicamente y, posiblemente, aceleradas por el calor o los metales. Más tarde, se desarrollaron enzimas primitivas, acelerando aún más esa química primordial de la vida.
A lo largo del tiempo geológico, la geoquímica se habría vuelto más rápida y elaborada, añadiendo nuevas reacciones. En algún momento del proceso, habrían surgido las membranas celulares y un sistema de herencia, en forma de ARN o ADN. La geoquímica se transformaría en bioquímica.
Esta segunda hipótesis carecía de pruebas experimentales clave hasta hace relativamente poco. Pero en los últimos años, investigadores han podido probar en el laboratorio vastas combinaciones de mezclas y condiciones químicas e identificar formas de replicar reacciones metabólicas básicas que tienen lugar en las células —todo ello sin enzimas—.
La idea de que la geoquímica precedió a la bioquímica es “una idea realmente poderosa”, afirma Susan Lang, geoquímica de la Woods Hole Oceanographic Institution en Massachusetts. “Y creo que [los científicos] han aportado muchas pruebas que respaldan esa idea”.
Orígenes inorgánicos
Ya en 1910, el biólogo ruso Konstantin Sergejewitch Mereschkowsky razonó que las primeras células tuvieron que producir moléculas orgánicas —la materia de la vida— a partir de sustancias inorgánicas. En concreto, tuvieron que tomar hidrógeno (H2) y dióxido de carbono (CO2) para fabricar moléculas orgánicas como ácidos grasos, azúcares y aminoácidos.
Hace unos 20 años, el microbiólogo evolutivo Bill Martin, de la Universidad de Düsseldorf, en Alemania, y el geoquímico Mike Russell, del Laboratorio de Propulsión a Chorro de la NASA, en California, propusieron que la vida comenzó en un lugar adecuado para estas reacciones críticas: las fuentes hidrotermales de las profundidades marinas.
Dentro de estas fumarolas hidrotermales, el hierro de la roca reacciona con el agua para producir hidrógeno. Y ese hidrógeno podría reaccionar con el CO2 para producir moléculas orgánicas simples que son fundamentales para la bioquímica celular: el formiato, con un átomo de carbono, el acetato con dos átomos de carbono y el piruvato con tres átomos de carbono.
Este vídeo, grabado durante una expedición del Schmidt Ocean Institute, captura la vida que bulle hoy en día alrededor de una fuente hidrotermal bajo el Océano Atlántico Norte. Hace eones, este podría haber sido el tipo de lugar donde la química de la vida tuvo su primer comienzo. El agua de las fuentes hidrotermales reacciona con el hierro de las rocas ricas en minerales y produce gas hidrógeno —que reacciona con el dióxido de carbono para producir pequeñas moléculas orgánicas—.
CRÉDITO: SCHMIDT OCEAN
Guiados por esta idea, en 2010 Lang y su equipo en Woods Hole, trabajando en la Ciudad Perdida, un campo hidrotermal en medio del Océano Atlántico, confirmaron que pequeñas moléculas orgánicas se producen en las fuentes, bastante separadas de la actividad de los microbios que viven en estos ambientes extremos.
Una vía microbiana
Los científicos también observaron que los pasos de estas reacciones geoquímicas en las fuentes hidrotermales son idénticos a la forma en que las células microbianas que viven cerca de las fuentes hidrotermales producen moléculas orgánicas a partir de CO2 e hidrógeno. Esto encaja perfectamente con la idea de que las vías bioquímicas comenzaron como reacciones geoquímicas, y las enzimas evolucionaron solo más tarde.
De hecho, Martin y sus colegas han demostrado que este conjunto particular de reacciones, conocido como la vía del acetil-CoA, es muy antiguo. Es compartido por dos grupos fundamentales de vida, las bacterias y las arqueas —y, por lo tanto, se remonta al último antepasado común de toda la vida en la Tierra—.
Pero las células microbianas actuales necesitan 127 enzimas para producir ese piruvato de tres carbonos. ¿Podrían los científicos replicar esta vía en un laboratorio, sin enzimas, como habría sido el caso en los albores de la vida? Martin, su entonces estudiante Martina Preiner, el químico Joseph Moran, ahora en la Universidad de Ottawa, Canadá, y sus colegas demostraron recientemente que en efecto podían hacerlo.
En uno de los informes, publicado en 2020, Preiner realizó pruebas en una serie de reactores químicos que podían soportar altas temperaturas. En estos recipientes introdujo dióxido de carbono, así como viales que contenían agua más hierro o níquel en diversas proporciones. Luego los dejó reaccionar durante la noche.

Este es el reactor químico que los investigadores Martina Preiner y Bill Martin utilizaron para poner a prueba si el agua, el dióxido de carbono y algunos metales eran suficientes para producir moléculas orgánicas.
CRÉDITO: BILL MARTIN
El gran avance de Preiner se produjo cuando se dio cuenta de que necesitaba hacer funcionar los reactores con un metal a la vez y controlar los niveles de hidrógeno presentes. Una vez hecho esto, los reactores produjeron de forma fiable formiato, acetato, piruvato, metanol y metano —todos ellos producidos por bacterias—.
“Estos metales sustituyen a 127 enzimas y nos dan cinco productos que son exactamente los productos de la vía biológica”, afirma Martin.
Los científicos señalan que el hierro y el níquel se encuentran en las fuentes hidrotermales de las profundidades marinas, donde podrían haber ayudado a dirigir las reacciones prebiológicas.
Además, estos metales todavía se encuentran en las partes de las enzimas modernas que catalizan la vía del acetil-CoA dentro de las células. “Los metales estaban allí primero, y luego las enzimas los incorporaron, pero los metales siguen siendo los catalizadores esenciales”, dice Martin.
Los metales abundaban en el planeta primigenio. El hierro, en particular, estaba en todas partes, afirma Markus Ralser, investigador del metabolismo en Charité - Universitätsmedizin de Berlín. “No se puede evitar la química del hierro, y por eso lo tenemos en todas partes en la química que se implementa en nuestras células”, afirma.
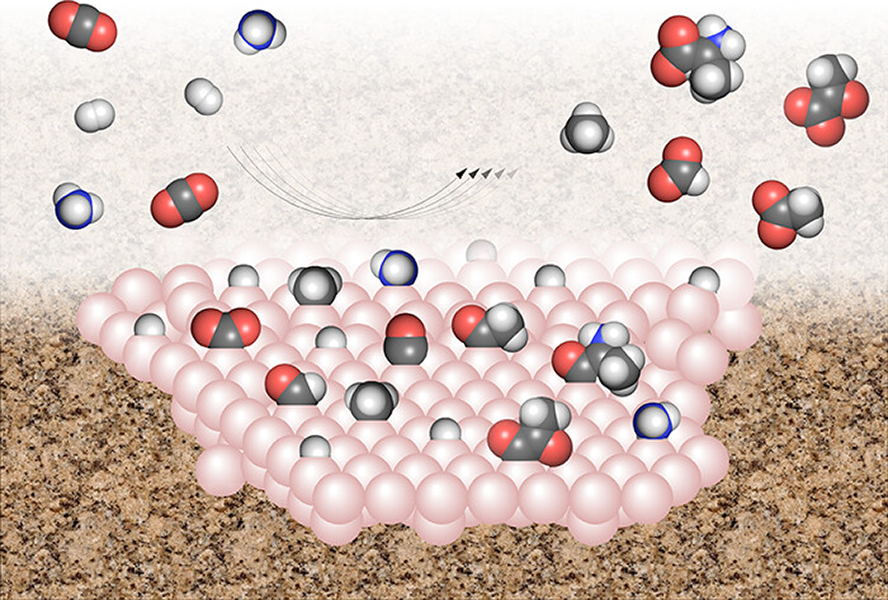
Las rocas de las fuentes hidrotermales contienen pequeñas estructuras en forma de burbuja llamadas poros hidrotermales. La síntesis de pequeñas moléculas orgánicas es catalizada por metales (círculos de color rosa) en las superficies minerales de estos poros. Quizás eventos como estos desencadenaron la evolución de la bioquímica primitiva.
CRÉDITO: N. MRNJAVAC ET AL / ACCOUNTS OF CHEMICAL RESEARCH 2024
Avanzando sin enzimas
El piruvato que Preiner, Martin y Moran fabricaron en sus experimentos es esencial para otra parte importante del metabolismo celular: la producción de aminoácidos y nucleótidos. Las células vivas necesitan aminoácidos para unirse y formar proteínas, y necesitan nucleótidos para producir ADN y ARN.
La línea de montaje central que fabrica estas sustancias se denomina ciclo del ácido tricarboxílico inverso, y el piruvato es uno de los elementos clave del ciclo.
Moran ha estado trabajando para replicar el ciclo del ácido tricarboxílico inverso fuera de las células durante la mayor parte de una década. Cuando empezó, los investigadores del origen de la vida tenían muchas ideas geniales, pero pocos estaban teniendo éxito en sus experimentos. Él quería aplicar su experiencia en catálisis química a cuestiones importantes en el campo.
El principal desafío, tal como lo veía Moran, era que, aunque las reacciones en ciclo del ácido tricarboxílico inverso son teóricamente posibles —lo que significa que las propiedades químicas las impulsarían en última instancia, como la gravedad favorecería una caminata cuesta abajo—, algunas de estas reacciones tardan muchísimo en iniciarse. Tienen lo que se llama una barrera de activación alta, como una pequeña colina que hay que subir antes de que pueda comenzar esa caminata cuesta abajo. ¿Sería posible superar estas barreras de activación sin enzimas? ¿Bajo qué condiciones?
“Mi forma de abordar el problema venía del mundo del desarrollo de la catálisis química y el cribado, que es: ‘no pensemos demasiado en ello, diseñemos algunos experimentos que se puedan realizar, en los que podamos realizar un gran número de experimentos en paralelo, y solo lo buscaremos empíricamente de una manera muy eficiente’”, dice Moran.
A partir de 2015, Moran y su equipo (entonces en la Universidad de Estrasburgo, en Francia, donde todavía realiza algunos trabajos) estudiaron cada una de las 11 reacciones principales del ciclo del ácido tricarboxílico inverso, probando todos los catalizadores metálicos y no orgánicos que pudieron conseguir, en todas las condiciones imaginables: a diferentes temperaturas y valores de pH, en presencia de diferentes metales y minerales.
Algunos tubos de ensayo intentarían completar el primer paso: la conversión de piruvato en oxaloacetato. Otros intentarían llevar a cabo la siguiente reacción, de oxaloacetato a malato. Y así sucesivamente. Además de las reacciones centrales en el ciclo del ácido tricarboxílico inverso, los científicos investigaron más recientemente las reacciones que se ramifican a partir de este ciclo para producir nucleótidos, aminoácidos y fosfatos de azúcar.
El equipo utilizó un mecanismo automatizado para analizar muestras las 24 horas del día, día tras día. “Solo lo hicimos durante tres años”, dice Moran.
En 2019, el equipo de Moran dio a conocer que podían producir nueve de los 11 metabolitos del ciclo del ácido tricarboxílico inverso sin enzimas. También identificaron las condiciones en las que seis de las 11 reacciones pueden funcionar juntas, en el mismo tubo de ensayo. “La gran mayoría de las reacciones y el metabolismo parecían lo suficientemente fáciles como para que pudieran producirse sin enzimas”, afirma Moran. “Al mismo tiempo, tenemos que ser realistas y decir que no hemos identificado ninguna condición que permita que surja un metabolismo completo; encontramos condiciones que permiten que ocurran pequeños tramos de él aquí, y reacciones específicas allá”.
Pero Moran es optimista sobre la posibilidad de recrear un metabolismo no enzimático. Solo se necesitará algo de creatividad para identificar las condiciones en las que pueden ocurrir algunas de las reacciones más complicadas, como la conversión de piruvato en oxaloacetato, afirma.
“Lo que Joseph hizo en la última década fue realmente extraordinario”, afirma Preiner, que ahora dirige un grupo de laboratorio en el Instituto Max Planck de Microbiología Terrestre en Marburgo, Alemania. “Eso fue una de las cosas más importantes que alguien ha hecho en los últimos 50 años, para el origen de la vida —ver realmente cómo ciertas reacciones pueden funcionar de forma no enzimática—”.
Pequeñas pero cruciales piezas que faltan
Mientras continúan su trabajo sobre el inicio de la química de la vida, Preiner y Moran se han centrado en pequeños productos químicos llamados cofactores o coenzimas, que ayudan en las reacciones enzimáticas.
Estos cofactores son extremadamente importantes. Uno llamado NAD+ transfiere electrones entre moléculas —una tarea crucial durante las reacciones— y otro llamado SAM toma y da grupos metilo a los productos químicos orgánicos que se están procesando. “Realizan tareas bastante simples, pero muy, muy, centrales e importantes del metabolismo”, dice Preiner. Es difícil imaginar que ellos o algún químico como ellos no estuvieran involucrados desde el principio, añade.
“Eso fue una de las cosas más importantes que alguien ha hecho en los últimos 50 años, para el origen de la vida —ver realmente cómo ciertas reacciones pueden funcionar de forma no enzimática—”
— MARTINA PREINER
Los científicos quieren saber qué papel podrían haber desempeñado estos cofactores en los albores de la vida y cómo se integraron en la geoquímica y, posteriormente, en la bioquímica.
Están descubriendo que los cofactores actuales pueden tener actividad catalítica, como una enzima. Y algunos incluso pueden catalizar su propia producción. Por lo tanto, tendría sentido, dice Moran, que estos cofactores hubieran sido cruciales para acelerar las reacciones metabólicas. Podrían haber acelerado algunas vías químicas sobre otras, ayudando a esculpir una red bioquímica.
Los científicos también piensan que algunos de esos cofactores tuvieron un papel en un paso fundamental en la evolución celular: la aparición de los genes. Un cofactor llamado NADH, señalan, consta de dos nucleótidos, los componentes básicos de los que están hechos el ARN y el ADN.
“Tal y como lo imagino ahora mismo, podría ser que estas moléculas, en una Tierra primitiva, se estuvieran produciendo en exceso. Y así se les asignaron diferentes tareas: algunas de ellas se incorporaron al ARN y otras al metabolismo”, afirma Preiner.
Los investigadores saben que, por supuesto, nunca podrán saber exactamente cómo surgió la vida: son como arqueólogos o paleontólogos que intentan reconstruir el pasado profundo a partir de escasas reliquias desmoronadas. De hecho, comenta Pascal, no había nada predeterminado en el metabolismo de la vida que persistiera y se impusiera entre muchos otros posibles sistemas químicos autocatalíticos. “Este resultado no es el único posible”, dice. “Tenemos muchas otras posibilidades”.
Aun así, los científicos han demostrado que es posible crear un metabolismo no enzimático que es asombrosamente similar al de los microbios en las fuentes hidrotermales, proporcionando pruebas clave y concretas para una idea teórica centenaria sobre los orígenes de la vida. Al igual que los fósiles en las rocas antiguas o los artefactos en las antiguas tumbas, las reacciones bioquímicas dentro de las células vivas nos conectan con una época mucho antes de que existiera la vida más primitiva en el planeta.
Artículo traducido por Debbie Ponchner
10.1146/knowable-050825-1
Apoye a la revista Knowable
Ayúdenos a hacer que el conocimiento científico sea accesible para todos
DONAREXPLORE MÁS | Lea artículos científicos relacionados