Las poderosas mitocondrias: las centrales energéticas de las células aprovechadas para la curación
La infusión de estas diminutas estructuras con forma de salchicha ayuda a rejuvenecer los tejidos privados de sangre. Los investigadores esperan que esta técnica pueda tratar diversos órganos dañados.
Manténgase informado
Suscríbase al boletín de noticias de Knowable en español
James McCully estaba en el laboratorio extrayendo unas estructuras diminutas llamadas mitocondrias de las células cuando investigadores de su equipo entraron corriendo. Habían estado operando un corazón de cerdo y no conseguían que volviera a bombear con normalidad.
McCully estudia la prevención de daños cardíacos en el Boston Children’s Hospital y la Facultad de Medicina de Harvard, y estaba muy interesado en las mitocondrias. Estos orgánulos productores de energía son especialmente importantes para órganos como el corazón, que tienen grandes necesidades energéticas. McCully se preguntaba si el trasplante de mitocondrias sanas a corazones dañados podría ayudar a restaurar su función.
El corazón del cerdo se estaba volviendo gris rápidamente, por lo que McCully decidió intentarlo. Llenó una jeringa con las mitocondrias extraídas y las inyectó directamente en el corazón. Ante sus ojos, este comenzó a latir con normalidad y recuperó su tono rosado.
Desde aquel día, hace casi 20 años, McCully y otros investigadores han replicado ese éxito en cerdos y otros animales. Los trasplantes en seres humanos fueron el siguiente paso, en bebés que sufrían complicaciones tras una cirugía cardíaca —lo que dio lugar a un nuevo campo de investigación que utiliza el trasplante de mitocondrias para tratar órganos dañados y enfermedades—. En los últimos cinco años, un número cada vez mayor de científicos ha comenzado a explorar el trasplante de mitocondrias para tratar daños cardíacos tras un paro cardíaco, daños cerebrales tras un accidente cerebrovascular y daños en órganos destinados a ser trasplantados.
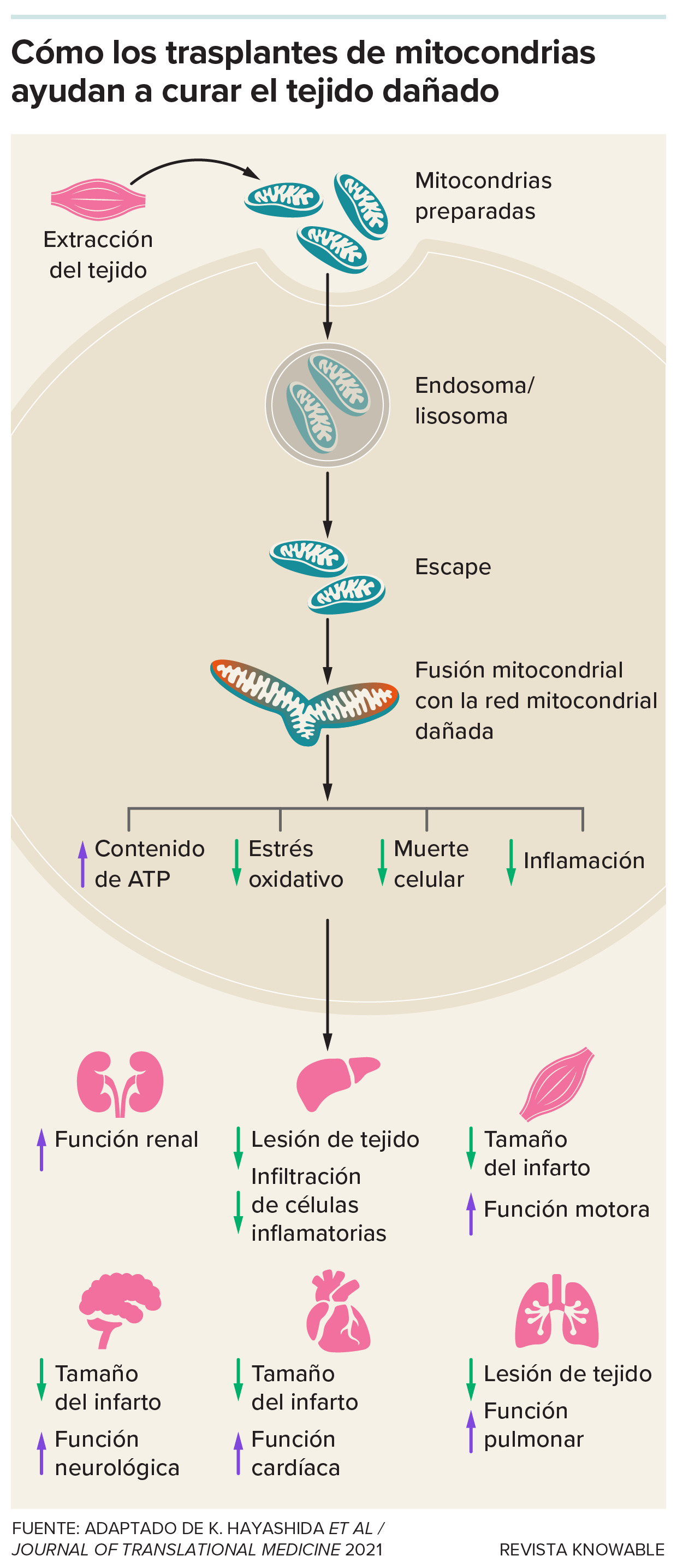
Este gráfico muestra los pasos básicos y los resultados del trasplante mitocondrial. Los científicos creen que las mitocondrias del donante se fusionan con las redes mitocondriales de las células receptoras. A continuación, actúan para reducir el tamaño del infarto (el área de tejido que muere por falta de sangre y oxígeno), entre otros efectos. Los científicos han estudiado estos trasplantes en riñones, hígados, músculos, cerebros, corazones y pulmones.
Las mitocondrias son más conocidas por producir energía utilizable para las células. Pero también envían señales moleculares que ayudan a mantener el equilibrio del cuerpo y a gestionar sus respuestas inmunitarias y al estrés. Algunos tipos de células pueden donar de forma natural mitocondrias sanas a otras células que las necesitan, como las células cerebrales tras un accidente cerebrovascular, en un proceso denominado transferencia mitocondrial. Por lo tanto, la idea de que los médicos pudieran potenciar este proceso mediante el trasplante de mitocondrias para revitalizar el tejido dañado tenía sentido para algunos científicos.
A partir de estudios en células cardíacas de conejos y ratas, el grupo de McCully ha encontrado que las membranas plasmáticas de las células envuelven las mitocondrias y las transportan al interior, donde se fusionan con las mitocondrias internas de la célula. Allí, parecen provocar cambios moleculares que ayudan a recuperar la función cardíaca: al comparar corazones de cerdos privados de sangre y oxígeno tratados con mitocondrias con otros que recibieron placebos, el grupo de McCully observó diferencias en la actividad de genes y proteínas que indicaban menos muerte celular y menos inflamación.
Hace unos 10 años, Sitaram Emani, cirujano cardíaco del Boston Children’s Hospital, se puso en contacto con McCully para informarse sobre su trabajo con corazones de animales. Emani había observado que algunos bebés con defectos cardíacos no se recuperaban completamente tras sufrir complicaciones en la cirugía cardíaca y se preguntaba si el método de trasplante de mitocondrias de McCully podría ayudarles.
Durante la cirugía para reparar defectos cardíacos, los cirujanos utilizan un fármaco para detener el corazón y poder operar. Pero si el corazón se ve privado de sangre y oxígeno durante demasiado tiempo, las mitocondrias comienzan a fallar y las células empiezan a morir, en una condición llamada isquemia. Cuando la sangre comienza a fluir de nuevo, en lugar de devolver el corazón a su estado normal, puede dañar y matar más células, lo que da lugar a una lesión por isquemia-reperfusión.
Dado que los ocho años de estudios de McCully en conejos y cerdos no habían revelado problemas de seguridad con el trasplante de mitocondrias, McCully y Emani pensaron que valía la pena probar el procedimiento en bebés con pocas posibilidades de recuperar la función cardíaca suficiente para dejar el soporte cardiopulmonar.
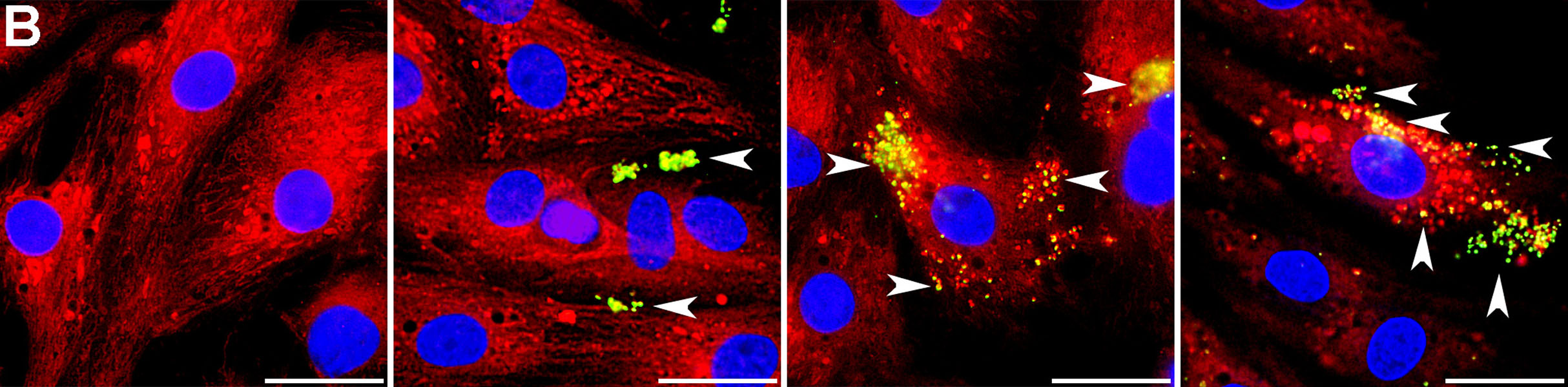
La imagen de la izquierda muestra células cardíacas de rata que no recibieron un trasplante. Las otras tres imágenes muestran (de izquierda a derecha): mitocondrias donadas (amarillo verdoso) fuera de las células cardíacas de rata dos horas después del trasplante; mitocondrias del donante dentro de las células ocho horas después; y mitocondrias del donante dentro y fuera de las células 24 horas después.
CRÉDITO: A. MASUZAWA ET AL / AMERICAN JOURNAL OF PHYSIOLOGY-HEART AND CIRCULATORY PHYSIOLOGY 2013
Los padres de 10 pacientes aceptaron someterse al procedimiento experimental, que fue aprobado por el comité de revisión del instituto. En un programa piloto que se llevó a cabo entre 2015 y 2018, McCully extrajo muestras de músculo del tamaño de un borrador de un lápiz de las incisiones realizadas para la cirugía cardíaca, utilizó una técnica de filtración para aislar las mitocondrias y comprobó que funcionaban. A continuación, el equipo inyectó los orgánulos en el corazón del bebé.
Ocho de esos 10 bebés recuperaron la función cardíaca suficiente para dejar de necesitar soporte vital, en comparación con solo cuatro de 14 casos similares entre 2002 y 2018 que se utilizaron para la comparación histórica, informó el equipo en 2021. El tratamiento también acortó el tiempo de recuperación, que fue de dos días en promedio en el grupo de trasplante mitocondrial, en comparación con nueve días en el grupo de control histórico. Dos pacientes no sobrevivieron: en un caso, la intervención se produjo después de que el resto de los órganos del bebé comenzaran a fallar y, en otro, se desarrolló un problema pulmonar cuatro meses después. El grupo ya ha realizado este procedimiento en 17 bebés.
El procedimiento de trasplante sigue siendo experimental y aún no es práctico para un uso clínico más amplio, pero McCully espera que algún día pueda utilizarse para tratar lesiones renales, pulmonares, hepáticas y de las extremidades causadas por la interrupción del flujo sanguíneo.
Los resultados han inspirado a otros médicos cuyos pacientes sufren lesiones similares por isquemia-reperfusión. Una de ellas es el ictus isquémico, en el que los coágulos impiden que la sangre llegue al cerebro. Los médicos pueden disolver o eliminar físicamente los coágulos, pero no disponen de ningún método para proteger el cerebro del daño causado por la reperfusión. “Ves pacientes que pierden la capacidad de caminar o hablar”, afirma Melanie Walker, neurocirujana endovascular de la Facultad de Medicina de la Universidad de Washington en Seattle. “Solo quieres hacerlo mejor y no hay nada que puedas hacer”.
Walker se topó con los estudios de trasplante mitocondrial de McCully hace 12 años y, al seguir leyendo, le llamó especialmente la atención un informe sobre ratones realizado por investigadores del Hospital General de Massachusetts y la Facultad de Medicina de Harvard que demostraba que las células de apoyo y protección del cerebro —los astrocitos— podían transferir parte de sus mitocondrias a las neuronas dañadas por un accidente cerebrovascular para ayudarlas a recuperarse. Quizás, pensó, el trasplante de mitocondrias también podría ayudar en casos de accidente cerebrovascular en humanos.
Pasó años trabajando con investigadores en animales para descubrir cómo administrar mitocondrias al cerebro de forma segura. Probó la seguridad del procedimiento en un ensayo clínico con solo cuatro personas con ictus isquémico: utilizando un catéter introducido a través de una arteria del cuello llegó a la obstrucción que causaba el ictus y la eliminó manualmente, luego, empujando el catéter más hacia dentro, liberó las mitocondrias, que viajaron por los vasos sanguíneos hasta el cerebro.
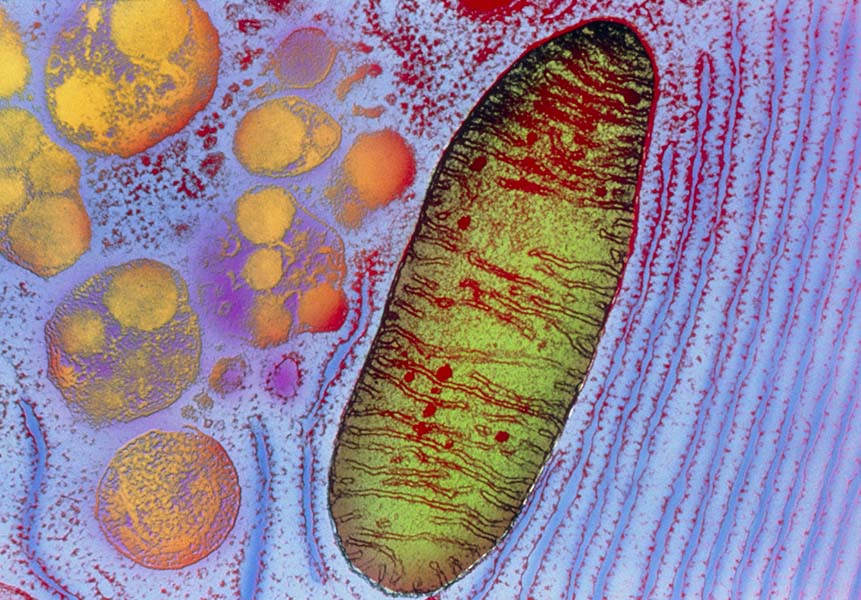
Además de ser las “centrales energéticas de la célula”, las mitocondrias participan en la regulación de otros procesos, como la muerte celular programada, la diferenciación celular y aspectos de la función inmunitaria.
CRÉDITO: KEITH R. PORTER / SCIENCE SOURCE
Los resultados, publicados en 2024 en la revista Journal of Cerebral Blood Flow & Metabolism, muestran que los pacientes a los que se les administró el tratamiento no sufrieron ningún daño; el ensayo no estaba diseñado para evaluar la eficacia. El grupo de Walker está reclutando participantes para evaluar más a fondo la seguridad de la intervención. El siguiente paso será determinar si las mitocondrias llegan a donde deben llegar y si funcionan. “Hasta que podamos demostrarlo, no creo que podamos afirmar que existe un beneficio terapéutico”, afirma Walker.
Los investigadores esperan que la donación de órganos también pueda beneficiarse de los trasplantes de mitocondrias. Los órganos donados, como los riñones, sufren daños cuando carecen de riego sanguíneo durante demasiado tiempo, y los cirujanos de trasplantes pueden rechazar los riñones con mayor riesgo de sufrir estas lesiones.
Para comprobar si los trasplantes mitocondriales pueden revitalizarlos, el cirujano y científico especialista en trasplantes Giuseppe Orlando, de la Facultad de Medicina de la Universidad Wake Forest en Winston-Salem, y sus colegas inyectaron mitocondrias en cuatro riñones de cerdo y una sustancia de control en otros tres. En 2023, en la revista Annals of Surgery, informaron de que había menos células muertas en los riñones tratados con mitocondrias y mucho menos daño. Los análisis moleculares también mostraron un aumento de la producción de energía.
Aún es pronto, afirma Orlando, pero confía en que el trasplante de mitocondrias pueda convertirse en una herramienta valiosa para rescatar órganos subóptimos para la donación.
Los estudios han suscitado tanto entusiasmo como escepticismo. “Sin duda, es un campo muy interesante”, afirma Koning Shen, bióloga mitocondrial postdoctoral de la Universidad de California, Berkeley, y coautora de una reseña sobre las funciones de señalización de las mitocondrias publicada en el Annual Review of Cell and Developmental Biology de 2022. Añade que ampliar la extracción de mitocondrias y aprender a almacenar y conservar los orgánulos aislados son los principales obstáculos técnicos para que estos tratamientos se conviertan en una realidad a mayor escala. “Sería increíble que se llegara a esa fase”, afirma.
“Creo que hay mucha gente inteligente estudiando esto detenidamente, pero creo que la gran pregunta es: ¿cuál es el mecanismo?”, afirma Navdeep Chandel, investigador de mitocondrias de la Universidad Northwestern en Chicago. Duda que las mitocondrias de los donantes reparen o sustituyan los orgánulos nativos disfuncionales, pero afirma que es posible que la donación de mitocondrias desencadene señales inmunitarias de estrés que benefician indirectamente al tejido dañado.
Sea cual sea el mecanismo, algunos estudios en animales sugieren que las mitocondrias deben ser funcionales para transmitir sus beneficios. Lance Becker, presidente de medicina de urgencias en Northwell Health, en Nueva York, que estudia el papel de las mitocondrias en el paro cardíaco, llevó a cabo un estudio en el que comparó mitocondrias frescas, mitocondrias que habían sido congeladas y luego descongeladas, y un placebo para tratar ratas tras un paro cardíaco. Las 11 ratas que recibieron mitocondrias frescas y funcionales tuvieron una mejor función cerebral y una mayor tasa de supervivencia tres días después que las 11 ratas que recibieron un placebo; las mitocondrias congeladas y descongeladas que no funcionaban no aportaron estos beneficios.
Según los investigadores, se necesitarán más investigaciones sobre los mecanismos de la terapia mitocondrial, mejores técnicas de administración de mitocondrias, ensayos más amplios y un conjunto de casos de éxito documentados antes de que los trasplantes mitocondriales puedan ser aprobados por la FDA y utilizarse ampliamente para tratar las lesiones por isquemia-reperfusión. El objetivo final sería crear un suministro universal de mitocondrias almacenadas, una especie de banco de mitocondrias, que pudiera ser utilizado para trasplantes por una amplia variedad de profesionales sanitarios.
“Estamos en una fase muy inicial, no sabemos cómo funciona”, afirma Becker. “Pero sabemos que está haciendo algo muy interesante”.
Artículo traducido por Debbie Ponchner
10.1146/knowable-081225-1
Apoye a la revista Knowable
Ayúdenos a hacer que el conocimiento científico sea accesible para todos
DONAREXPLORE MÁS | Lea artículos científicos relacionados